Difference between revisions of "Lei de Boyle-Mariotte"
m |
(Imagens e remoção de sec. colapsáveis.) |
||
| Line 1: | Line 1: | ||
| − | + | =Descrição da experiência= | |
O propósito desta experiência é a verificação da relação \( p \propto \frac{1}{V} \) (ou seja, que a pressão e o volume são inversamente proporcionais) de um gás durante uma compressão ou expansão isotérmica | O propósito desta experiência é a verificação da relação \( p \propto \frac{1}{V} \) (ou seja, que a pressão e o volume são inversamente proporcionais) de um gás durante uma compressão ou expansão isotérmica | ||
| − | + | ||
| − | + | =Aparato experimental= | |
| − | |||
A montagem consiste num cilindro cheio de ar, cujo êmbolo é actuado por um servo motor (o par cilindro/êmbolo é implementado com uma seringa de 5cc). | A montagem consiste num cilindro cheio de ar, cujo êmbolo é actuado por um servo motor (o par cilindro/êmbolo é implementado com uma seringa de 5cc). | ||
| − | [ | + | [[File:Boyle-mariotte-montagem.jpg|thumb|alt=Montagem Boyle-Mariotte|Montagem]] |
| + | |||
| + | É possível escolher os limites da compressão ou expansão do pistão e obter dados referentes ao curso do mesmo (volume) e da pressão a que se encontra o ar no interior do cilindro. A velocidade a que se desenrola a experiência também pode ser especificada escolhendo o tempo entre aquisições, podendo-se assim observar o desvio em relação à lei de Boyle-Mariotte se se escolher uma compressão ou expansão demasiado rápidas. | ||
| − | |||
| − | |||
| − | + | =Protocolo= | |
| − | |||
| − | |||
Os paramatros a definir são o volume inicial e final, o número de amostras e o tempo entre amostras. | Os paramatros a definir são o volume inicial e final, o número de amostras e o tempo entre amostras. | ||
Se se executar a experiência com um tempo elevado entre amostras, estará a efectuar uma experiência isotérmica, ou seja, a temperatura do ar no êmbolo é aproximadamente constante e por isso a lei de Boyle-Mariotte verifica-se. O exemplo seguinte é um caso desses, onde se pode verificar que o produto \( pV \) é em média, \( 49,3 \pm 0,3 L.kPa \), aproximado ao valor teórico de \( nRT \) (considerando \( n = 2 \times 10 ^{-4} mol \), equivalente ao volume da seringa cheia e em repouso, ou seja \( 5 ml \), PTN). | Se se executar a experiência com um tempo elevado entre amostras, estará a efectuar uma experiência isotérmica, ou seja, a temperatura do ar no êmbolo é aproximadamente constante e por isso a lei de Boyle-Mariotte verifica-se. O exemplo seguinte é um caso desses, onde se pode verificar que o produto \( pV \) é em média, \( 49,3 \pm 0,3 L.kPa \), aproximado ao valor teórico de \( nRT \) (considerando \( n = 2 \times 10 ^{-4} mol \), equivalente ao volume da seringa cheia e em repouso, ou seja \( 5 ml \), PTN). | ||
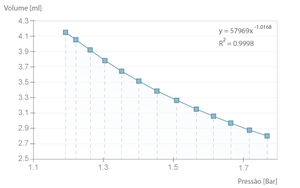
| − | [ | + | [[File:Boyle-mariotte-graf1.png|thumb|Ajuste experimental aos dados de uma aquisição efectuada com 1 s entre amostras]] |
| + | |||
| + | No caso de se diminuir o tempo entre amostras, o comportamento da compressão do ar deixa de ser isotérmico e passa a aproximar-se de adiabático, uma vez que não existe tempo para trocas de calor entre o ar no interior do cilindro e o meio ambiente. Desta forma a compressão afasta-se da lei de Boyle-Mariotte, claramente demonstrado pelo desvio da potência de ajuste, que no caso ideal seria \( ^3/_5 \) ( \( \gamma ^{-1} = \frac{c_v}{c_p} \) ). No entanto, é muito difícil obter uma rapidez de compressão que permita obter este valor, pois a termalização é muito rápida (dá-se na ordem da velocidade do som). | ||
| − | |||
| − | |||
| − | + | =Protocolo Avançado= | |
| − | |||
| − | |||
Com um tempo entre amostras elevado, é também possível determinar o valor da constante dos gases perfeitos considerando que a temperatura ambiente é de 22ºC. | Com um tempo entre amostras elevado, é também possível determinar o valor da constante dos gases perfeitos considerando que a temperatura ambiente é de 22ºC. | ||
| + | |||
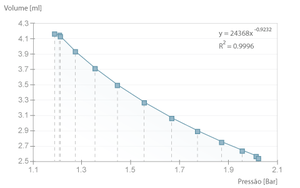
| + | [[File:Boyle-mariotte-graf2.png|thumb|Ajuste a uma experiência cujo tempo entre amostras é muito breve (5 ms), demonstrado o desvio da situação ideal (onde o expoente seria -1]] | ||
Como proceder: | Como proceder: | ||
| Line 34: | Line 31: | ||
# Assuma que a temperatura da sala é de 22ºC. Determine o número de moles presentes no início da experiência ( \( 5 ml \) de ar a PTN). Calcule \( R \). | # Assuma que a temperatura da sala é de 22ºC. Determine o número de moles presentes no início da experiência ( \( 5 ml \) de ar a PTN). Calcule \( R \). | ||
# Compare o valor de \( R \) determinado desta forma com o obtido através do valor médio do produto de \( pV \) (calculando no Excel o produto \( pV \) para cada linha e efectuando posteriormente a sua média) | # Compare o valor de \( R \) determinado desta forma com o obtido através do valor médio do produto de \( pV \) (calculando no Excel o produto \( pV \) para cada linha e efectuando posteriormente a sua média) | ||
| − | # Faça uma última estimativa de \( R \) forçando o expoente a (-1), ou seja ajustando uma função \( a x ^{-1} \). | + | # Faça uma última estimativa de \( R \) forçando o expoente a (-1), ou seja ajustando uma função \( a x ^{-1} \). |
| − | + | ||
| + | |||
| + | =Análise de Dados= | ||
| + | Em construção. | ||
| + | |||
| + | |||
| + | =Princípios Teóricos= | ||
| + | Em construção. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | =Elementos Históricos= | |
| − | + | Em construção. | |
| − | |||
| − | Em construção. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | =Bibliografia= | |
Em construção. | Em construção. | ||
Revision as of 16:24, 26 March 2012
Contents
Descrição da experiência
O propósito desta experiência é a verificação da relação \( p \propto \frac{1}{V} \) (ou seja, que a pressão e o volume são inversamente proporcionais) de um gás durante uma compressão ou expansão isotérmica
Aparato experimental
A montagem consiste num cilindro cheio de ar, cujo êmbolo é actuado por um servo motor (o par cilindro/êmbolo é implementado com uma seringa de 5cc).
É possível escolher os limites da compressão ou expansão do pistão e obter dados referentes ao curso do mesmo (volume) e da pressão a que se encontra o ar no interior do cilindro. A velocidade a que se desenrola a experiência também pode ser especificada escolhendo o tempo entre aquisições, podendo-se assim observar o desvio em relação à lei de Boyle-Mariotte se se escolher uma compressão ou expansão demasiado rápidas.
Protocolo
Os paramatros a definir são o volume inicial e final, o número de amostras e o tempo entre amostras.
Se se executar a experiência com um tempo elevado entre amostras, estará a efectuar uma experiência isotérmica, ou seja, a temperatura do ar no êmbolo é aproximadamente constante e por isso a lei de Boyle-Mariotte verifica-se. O exemplo seguinte é um caso desses, onde se pode verificar que o produto \( pV \) é em média, \( 49,3 \pm 0,3 L.kPa \), aproximado ao valor teórico de \( nRT \) (considerando \( n = 2 \times 10 ^{-4} mol \), equivalente ao volume da seringa cheia e em repouso, ou seja \( 5 ml \), PTN).
No caso de se diminuir o tempo entre amostras, o comportamento da compressão do ar deixa de ser isotérmico e passa a aproximar-se de adiabático, uma vez que não existe tempo para trocas de calor entre o ar no interior do cilindro e o meio ambiente. Desta forma a compressão afasta-se da lei de Boyle-Mariotte, claramente demonstrado pelo desvio da potência de ajuste, que no caso ideal seria \( ^3/_5 \) ( \( \gamma ^{-1} = \frac{c_v}{c_p} \) ). No entanto, é muito difícil obter uma rapidez de compressão que permita obter este valor, pois a termalização é muito rápida (dá-se na ordem da velocidade do som).
Protocolo Avançado
Com um tempo entre amostras elevado, é também possível determinar o valor da constante dos gases perfeitos considerando que a temperatura ambiente é de 22ºC.
Como proceder:
- Efectue uma experiência com algumas aquisições (p. ex. 20), uma excursão máxima entre volume inicial e final e o tempo de aquisição máximo permitido (situação da expansão isotérmica).
- Efectue um ajuste genérico do tipo \( a x ^b \) (utilizando o Excel ou o Origin p. ex.) aos dados experimentais e determine a constante de proporcionalidade que será igual a \( nRT \).
- Assuma que a temperatura da sala é de 22ºC. Determine o número de moles presentes no início da experiência ( \( 5 ml \) de ar a PTN). Calcule \( R \).
- Compare o valor de \( R \) determinado desta forma com o obtido através do valor médio do produto de \( pV \) (calculando no Excel o produto \( pV \) para cada linha e efectuando posteriormente a sua média)
- Faça uma última estimativa de \( R \) forçando o expoente a (-1), ou seja ajustando uma função \( a x ^{-1} \).
Análise de Dados
Em construção.
Princípios Teóricos
Em construção.
Elementos Históricos
Em construção.
Bibliografia
Em construção.